Depuis le début de la crise sanitaire majeure née du changement de formule du LEVOTHYROX, MERCK, l'ANSM et la ministre de la santé tiennent le même discours : en février 2012, à la suite d'une enquête officielle de pharmacovigilance, et pour limiter les différences de teneur en substance active selon les lots de la spécialité, l'Agence française de sécurité sanitaire des produits de santé a demandé à la société Merck Santé, titulaire des autorisations de mise sur le marché des spécialités Levothyrox, d'en restreindre les spécifications de teneur en lévothyroxine sodique dans les limites de 95/105 % de la dose déclarée sur toute la durée de vie du produit. A cette fin, la société a sollicité un changement de la formule de ses spécialités, consistant en la modification des excipients utilisés, qui a été autorisée le 27 septembre 2016 par l'Agence nationale de sécurité du médicament et des produits de santé, au vu de deux études de pharmacocinétique démontrant la bioéquivalence de l'ancienne et de la nouvelle formules.
En effet, le discours officiel consiste à rappeler que jusqu'en 2017, l'ancienne formule du LEVOTHYROX comprenait de 90 à 111 % de principe actif ce qui aurait été une source d'instabilité du produit.
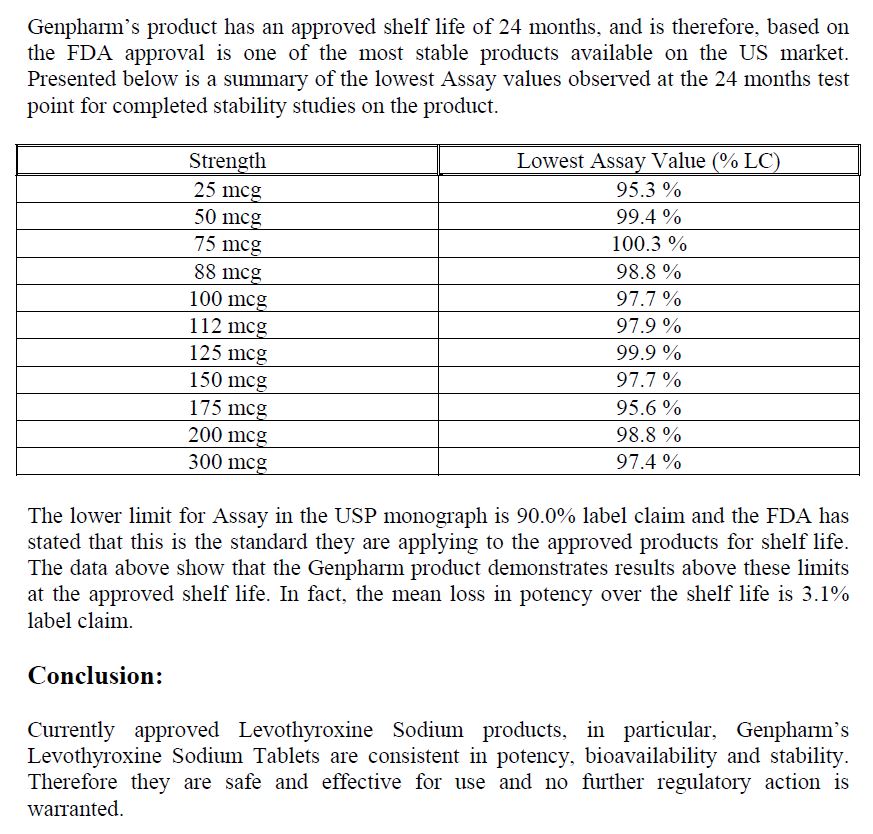
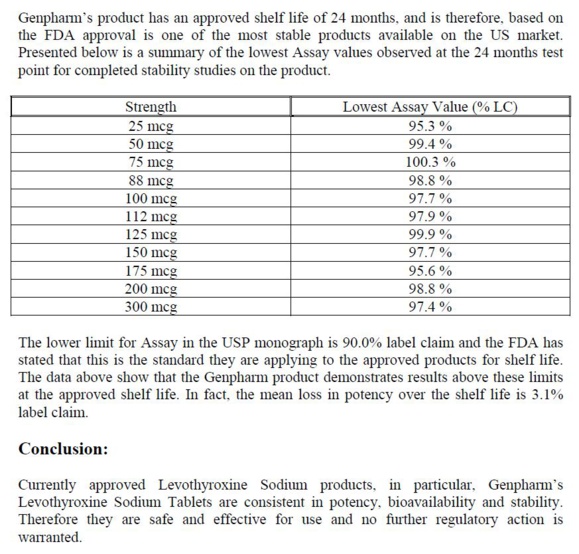
Pourtant, en 2005, devant la puissante FDA (Food & drug administration), MERCK et sa filiale nord américaine (GENPHARM) expliquait la lévothyroxine sodique commercialisée aux USA sous le nom de NOVOTHYROX était fabriquée en Allemagne et ne se distinguait pas des produits commercialisés sous d'autres noms, si ce n'est l'ajout d'un colorant alimentaire dans les comprimés.
Or, MERCK et GENPHARM se vantaient que le NOVOTHYROX respectait la norme 95 / 105 % de principe actif.
D'un point de vue industriel, il parait difficile d'admettre qu'une même usine produise le même médicament avec des process de fabrication affectant la teneur en principe actif, surtout quand les quantités sont malaisées à doser puisque l'on parle en microgramme (en millionième de gramme).
Restons prudents mais tous les ingrédients d'un SCANDALE SANITAIRE sont à présents réunis. Mme BUZYN devrait descendre de sa tour d'ivoire, rencontrer, écouter les malades et prendre la seule décision nécessaire : réquisitionner la production et la distribution du LEVOTHYROX avec lactose.
En effet, le discours officiel consiste à rappeler que jusqu'en 2017, l'ancienne formule du LEVOTHYROX comprenait de 90 à 111 % de principe actif ce qui aurait été une source d'instabilité du produit.
Pourtant, en 2005, devant la puissante FDA (Food & drug administration), MERCK et sa filiale nord américaine (GENPHARM) expliquait la lévothyroxine sodique commercialisée aux USA sous le nom de NOVOTHYROX était fabriquée en Allemagne et ne se distinguait pas des produits commercialisés sous d'autres noms, si ce n'est l'ajout d'un colorant alimentaire dans les comprimés.
Or, MERCK et GENPHARM se vantaient que le NOVOTHYROX respectait la norme 95 / 105 % de principe actif.
D'un point de vue industriel, il parait difficile d'admettre qu'une même usine produise le même médicament avec des process de fabrication affectant la teneur en principe actif, surtout quand les quantités sont malaisées à doser puisque l'on parle en microgramme (en millionième de gramme).
Restons prudents mais tous les ingrédients d'un SCANDALE SANITAIRE sont à présents réunis. Mme BUZYN devrait descendre de sa tour d'ivoire, rencontrer, écouter les malades et prendre la seule décision nécessaire : réquisitionner la production et la distribution du LEVOTHYROX avec lactose.


 Un avocat ?
Un avocat ?